جدول المحتويات
ما الوحدة الأساسية لتكوين المركبات التساهمية التي ترتبط فيما بينها بروابط تساهمية، حيث تختلف المركبات التساهمية عن المركبات الايونية في العديد من الخصائص بالإضافة إلى تركيبهما، لذلك من هذاالمنطلق سنتناول في هذه المقالة المركبات التساهمية، و ما الوحدة الأساسية لتكوين المركبات التساهمية.
المركبات التساهمية
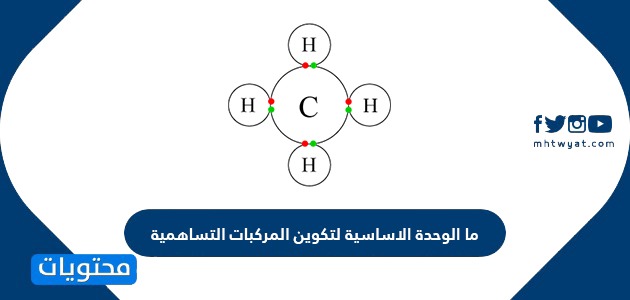
المركبات التساهمية شائعة جدًا فهي موجودة في الهواء الذي نتنفسه، والغاز الذي يتم استخدامه لتزويد السيارات بالوقود، والماء الذي يتم شربه، وحتى الطعام الذي يتم تناوله، كما ويتكون المركب التساهمي عندما تترابط ذرتان أو أكثر من الذرات اللافلزية عن طريق مشاركة إلكترونات التكافؤ، واللافلزات هي أنواع من العناصر تفتقر إلى الخصائص المعدنية أو الفلزية؛ وعادة ما تكون غازات في درجة حرارة الغرفة وهي موصلة رديئة للحرارة والكهرباء كما وتكتسب إلكترونات لتكوين أيونات سالبة، وتوجد اللافلزات في أقصى يمين الجدول الدوري، بالإضافة إلى أن الهيدروجين هو أيضًا مادة لافلزية، على الرغم من أنه يوجد في أعلى يسار الجدول الدوري؛ أما بالنسبة لإلكترونات التكافؤ هي الإلكترونات الأبعد عن الذرة، وتتشارك هذه الإلكترونات في الترابط لوصولها للاستقرار، وذلك بأن يكون في غلافها الأخير ثماني إلكترونات، بالتالي فإن إلكترونات التكافؤ تلعب دورًا حاسمًا في تكوين المركبات التساهمية، وتسمى عملية إرتباط إلكترونات التكافؤ المشتركة بين ذرتين غير فلزيتين بالرابطة التساهمية، كما ويُعرف إلكترونان مشتركان برابطة تساهمية أحادية، وتُعرف أربعة إلكترونات مشتركة باسم الرابطة التساهمية الثنائية، وستة الإلكترونات المشتركة تُعرف باسم الرابطة الثلاثية، والأكسجين الذي نتنفسه مثال على الرابطة التساهمية الثنائية، بينما غاز الميثان مثال على الرابطة التساهمية الأحادية. [1]
ما الوحدة الأساسية لتكوين المركبات التساهمية
تنقسم الروابط الكيميائية عمومًا والتي تربط مكونات المادة مع بعضها البعض عادة إلى نوعين مختلفين وهما الرابطة التساهمية والرابطة الأيونية، كما وأن للأنواع المختلفة من الروابط الكيميائية خصائص مختلفة جدًا، إذ تتكون المركبات الأيونية من أيونات موجبة وسالبة الشحنة مرتبطة ببعضها البعض بواسطة قوى كهروستاتيكية قوية، بينما تتكون المركبات التساهمية عمومًا من جزيئات، وهي مجموعات من الذرات يتم فيها مشاركة زوج واحد أو أكثر من الإلكترونات بين الذرات المترابطة، فبذلك تم الإجابة على السؤال المهم وهو ما الوحدة الأساسية لتكوين المركبات التساهمية وهي الجزيئات، كما أن في الرابطة التساهمية ترتبط الذرات ببعضها البعض عن طريق التجاذب الكهروستاتيكي بين النوى الموجبة الشحنة للذرات المترابطة، والإلكترونات سالبة الشحنة التي تشترك معها فيها. [2]
خصائص المركبات التساهمية
وبعد التعرف على إجابة ما الوحدة الأساسية لتكوين المركبات التساهمية ، من المهم التعرف على أهم خصائص المركبات التساهمية وهي كالآتي: [3]
درجات الانصهار و درجات الغليان
تحتوي معظم المركبات التساهمية على درجات انصهار ودرجات غليان منخفضة نسبيًا، حيث عندما تنجذب الأيونات الموجودة في المركب الأيوني بقوة لبعضها البعض فهي تحتاج إلى طاقة كبيرة لفصلها، وبالتالي درجان غليان وانصهار عالية جدًا، لكن في المقابل الروابط التساهمية تكون جزيئات يمكن أن تنفصل عن بعضها البعض عند إضافة أقل كمية من الطاقة إليها.
طرية ومرنة
تميل المركبات التساهمية إلى أن تكون طرية ومرنة تقريبًا، ويرجع ذلك إلى أن الروابط التساهمية مرنة نوعًا ما ويسهل كسرها، كما وتؤدي الروابط التساهمية في المركبات الجزيئية إلى تكوين هذه المركبات على شكل غازات وسوائل ومواد صلبة ناعمة، ولكن المركبات الجزيئية البلورية لا تنطبق عليها هذه الخاصية، حيث أنها صلبة وليست طرية ومرنة.
قابلة للاشتعال
تميل المركبات التساهمية إلى أن تكون أكثر قابلية للاشتعال من المركبات الأيونية، حيث تحتوي العديد من المواد القابلة للاشتعال في وقتنا الراهن على ذرات الهيدروجين والكربون التي يمكن أن تتعرض للاحتراق، حيث أن الاحتراق تفاعل يطلق الطاقة عندما يتفاعل المركب مع الأكسجين لإنتاج ثاني أكسيد الكربون والماء، كما أن كهروسالبية الكربون والهيدروجين متشابهة نوعًا ما لذلك يوجدان معًا في العديد من المركبات الجزيئية.
غير موصلة للتيار الكهربائي
المركبات التساهمية عند إذابتها في الماء لا توصل الكهرباء، حيث أن المركبات الجزيئية تتحلل إلى جزيئات بدلاً من أن تنفصل إلى أيونات عند إذابتها في الماء، لذا فهي عادةً لا توصل الكهرباء بشكل جيد.
ذوبانها في الماء
العديد من المركبات التساهمية عبارة عن جزيئات قطبية تذوب جيدًا في مذيب قطبي ، مثل الماء، ومن أمثلة المركبات الجزيئية التي تذوب جيدًا في الماء السكر والإيثانول، بينما العديد من المركبات التساهمية لا تذوب جيدًا في الماء، ومن أمثلة المركبات الجزيئية التي لا تذوب جيدًا في الماء الزيت والبلاستيك المبلمر.
وفي ختام هذه المقالة نلخص لأهم ما جاء فيها من عناوين، وذلك من توضيح المركبات التساهمية ، والإجابة على سؤال ما الوحدة الأساسية لتكوين المركبات التساهمية وهي الجزيئات المرتبطة مع بعضها البعض بروابط تساهمية، بالإضافة إلى ما تم عرضه في هذه المقالة هو أهم خصائص المركبات التساهمية مثل ذوبانها في الماء وتوصيلها للكهرباء، وغيرها.
المراجع
- ^ study.com , Covalent Compounds: Properties, Naming & Formation , 22/11/2020
- ^ wou.edu , Chapter 4 – Covalent Bonds and Molecular Compounds , 22/11/2020
- ^ thoughtco.com , Covalent or Molecular Compound Properties , 22/11/2020