جدول المحتويات
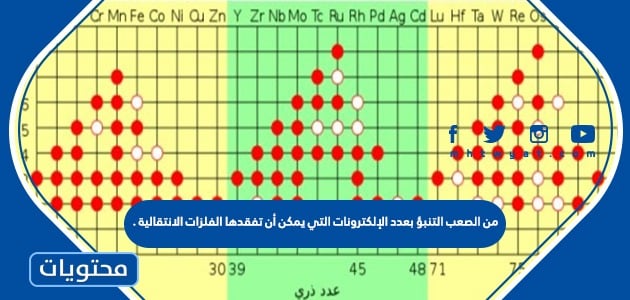
من الصعب التنبؤ بعدد الإلكترونات التي يمكن أن تفقدها الفلزات الانتقالية . العناصر الانتقالية هي مجموعة العناصر التي تشغل الأعمدة الموجودة في وسط الجدول الدوري، وتأخذ المستوى d، وسيقدم موقع محتويات في هذا المقال كافة المعلومات حول خصائص هذه العناصر، وأنواع الروابط الكيميائية.
أنواع الروابط الكيميائية
الروابط الكيميائية عبارة عن قوى تربط بين الذرات، وتقسم إلى:[1]
- الروابط الأيونية: وهي الأكثر قوة، يتم فيها نقل الإلكترون من ذرة إلى أخرى.
- الروابط التساهمية: وهي الأكثر شيوعاً، تساهم في تكوين الجزيء.
- الروابط التساهمية القطبية: روابط متوسطة بين الأيونية والتساهمية.
- الروابط الهيدروجينية: أقل قوة من الروابط الأيونية.
من الصعب التنبؤ بعدد الإلكترونات التي يمكن أن تفقدها الفلزات الانتقالية .
من الصعبِ التنبؤ بعدد الإلكترونات التي يُمكن أن تفقدَها الفلزات الانتقاليّة، العبارة صحيحة، ويعبر مصطلح العناصر الانتقالية على العناصر الكيميائية التي تحمل إلكترون تكافؤ، وتمثل العناصر الكيميائية الأربعين في الجدول الدوري من 21 إلى 29، ومن 39 إلى 47، ومن 71 إلى 79، ومن 103 إلى 111.[2]
شاهد أيضاً: تم ترتيب العناصر في الجدول الدوري بناء على.
خصائص العناصر الانتقالية
تمتلك العناصر الانتقالية مجموعة كبيرة من الخصائص، وأهمها:
- تتميز أنها معدنية، وتتمتع بالصلابة والقوة.
- امتلاكها درجة غليان ودرجة انصهار عاليتين، باستثناء الزئبق.
- موصلات جيدة للحرارة والكهرباء.
- تستخدم في مجال التكنولوجيا.
- يذوب معظمها بالأحماض.
- مرنة، يسهل طرقها وتشكيلها.
- طاقة تأين قليلة.
وفي ختام المقال من الصعبِ التنبؤ بعَدد الإلكترونات التي يُمكن أن تفقدَها الفلزات الانتقاليّة، تم التعرف أنواع الروابط الكيميائية، وتم التعرف على خصائص العناصر الانتقالية، كما تم التذكير بالأرقام الخاصة بها في الجدول الدوري.
المراجع
- ^ marefa.org , رابطة كيميائية , 13/10/2022
- ^ marefa.org , الجدول الدوري , 13/10/2022