جدول المحتويات
كم عدد عناصر الجدول الدوري يُعد من الأمور الهامة والأساسية في علم الكيمياء وتصنيف العناصر الكيميائية وفقًا لعدد كبير من الخصائص التي تختلف من مجموعة كيميائية إلى أخرى ومن عنصر إلى آخر، وعند البدء في دراسة علم الكيمياء؛ لا بُد أن يكون الطالب على علم ودراية بعدد عناصر وخواص الجدول الدوري وطريقة استخدامه للكشف عن العناصر بشكل صحيح، ومن هذا المنطلق؛ فإن السطور التالية سوف تتحدث تفصيليًا عن كل ما يخص الجدول الدوري.
كم عدد عناصر الجدول الدوري
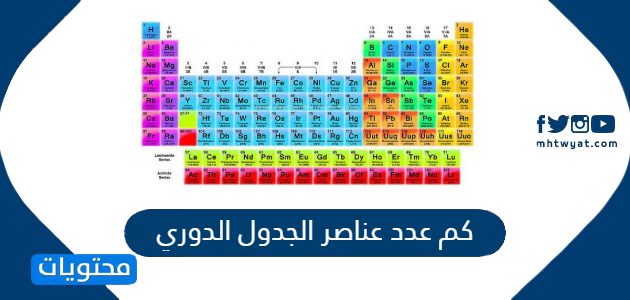
يحتوي الجدول الدوري على عدد هائل من العناصر أشار العلماء إلى أن عددها يبلغ 118 عنصرًا، حيث قد تم ترتيب تلك العناصر وترقيمها وفقًا للعدد الذري لكل منها والذي يُشير إلى عدد البروتونات الموجودة في نواة الذرة لكل عنصر، وتبدأ هذه العناصر بأصغرها من حيث العدد الذري وهو عنصر الهيدروجين ورقمه الذري 1، وتنتهي بعنصر أوغانيسون الذي يحمل عددًا ذريًا وعدد بروتونات يبلغ 118 ورمزه Uuo، وتتدرج الصفات والخصائص الخاصة بالعناصر داخل الجدول عند الاتجاه من اليسار إلى اليمين [1].
اقرأ أيضًا: الجدول الدوري
نظام الجدول الدوري
تم ترتيب العناصر في الجدول الدوري في صورة 18 مجموعة رأسية و7 دورات أفقية، وكل مجموعة أفقية تحتوي على العناصر التي تحمل نفس عدد الإلكترونات في مدار الطاقة الخارجي لها، وبالتالي؛ فإن خواصها الكيميائية تكون متشابهة، مما يُعني أن عناصر المجموعة الواحدة متشابهة إلى حد كبير في مساراتها داخل التفاعلات الكيميائية، وينقسم الجدول إلى أكثر من نوع من المجموعات غير أن معظم العناصر معدنية وغير معدنية.
ومن خلال التوزيع الإلكتروني لإلكترونات أي عنصر؛ يُمكن تحديد موقعه بالجدول الدوري، وعلى سبيل المثال عنصر الصوديوم وعدده الذري 11، فإن التوزيع الإلكتروني له سوف يتم خلال 3 مستويات طاقة هي K, L, M، وسوف يكون التوزيع 2, 8, 1 بالترتيب، وهذا يُعني أن توزيع هذا العنصر شمل 3 مستويات طاقة أي أنه يقع في الدورة رقم 3، والمستوى الأخير به إلكترون واحد؛ أي أنه يقع في المجموعة رقم واحد، وهكذا [2].
خواص الجدول الدوري
في ضوء استعراض العناصر وترتيبها في الجدول الدوري بالاعتماد على الأعداد الذرية؛ أشار العلماء إلى أن مجموعات الجدول تتميز ببعض الخصائص الملحوظة، مثل:
- تحتوي أول ثلاثة مجموعات من الجدول الدوري على الفلزات ذات القدرة على فقد إلكترون أو أكثر من مدارها الخارجي والتحول إلى أيون موجب، في حين أن عناصر باقي المجموعات تميل إلى اكتساب إلكترونات.
- تنتهي كل دورة من دورات الجدول الدوري بعنصر خامل، والعنصر الخامل هو العنصر المستقر الذي لا يميل إلى الدخول في التفاعلات الكيميائية نظرًا إلى أن مداره الخارجي يكون مكتملًا بالإلكترونات.
- من خلال الجدول؛ تم تقسيم العناصر إلى ثلاثة أنواع مختلفة هي: الفلزات، وأشباه الفلزات، واللافلزات، ولكل منهم خواص مختلفة تميزها.
اقرأ أيضًا: اسهامات الكيميائيين في تعرف خصائص الاحماض والقواعد
تاريخ الجدول الدوري
لقد مر الجدول الدوري بعدة مراحل من التطوير والتعديل وإضافة المزيد من العناصر الحديثة إليه إلى أن وصل إلى الشكل المتعارف عليه في وقتنا الحالي، حيث قد تم وضع الجدول الدوري لأول مرة بواسطة العالم مندليف في عام 1869م بالاعتماد على الكتل الذرية للعناصر، وفي عام 1863، وفي عام 1913م؛ تمكن العالم موزلي من اكتشاف علاقة بين تصوير الأشعة السينية للعناصر والعدد الذري، وبالتالي؛ تم تقدير الأعداد الذرية بشكل صحيح وبناء الجدول الدوري الجديد بترتيب العناصر على أساس أعدادها الذرية.
ويُذكر أن ما جعل نموذج موزلي هو الأفضل؛ هو تنبؤ العالم بظهور عناصر جديدة مع مرور الزمن وترك مكانًا فارغًا لها بالجدول، وعلى سبيل المثال؛ حينذاك لم يكن قد تم اكتشاف العناصر التي تحمل أعداد ذرية 61، 43، وعندما تم اكتشافها بعد ذلك تمكن العلماء من إضافتها إلى الجدول الدوري بسهولة.
مجموعات الجدول الدوري
في ضوء كم عدد عناصر الجدول الدوري فإن الجدول الدوري يحتوي على 18 مجموعة رأسية تشمل ما يلي:
- مجموعة فلزات قلوية.
- مجموعة تشمل على فلزات المعادن (الأرضية).
- مجموعتي اللانثانيدات والأكتنيدات وكل منهما تضم عناصر انتقالية فس سلسلتين أسفل الجدول، وبهما عدد من العناصر مختلف من باقي المجموعات.
- مجموعة المعادن الانتقالية.
- مجموعة المعادن (بعد الانتقالية).
- مجموعة تضم عناصر اللافلزات.
- مجموعة رقم 17 تضم الهالوجينات وأهم تلك العناصر: (الكلور، البروم، الفلور، اليود).
- مجموعة رقم 18 وهي تحتوي على الغازات الخاملة (النبيلة) التي لا تميل إلى الدخول في التفاعل الكيميائي.
الجدول الدوري للعناصر الكيميائية doc
من المؤكد أن الكثيرين من لطلبة والطالبات يسعون إلى الحصول على نسخة من الجدول الدوري الأصلي والأساسي حتى يتمكنوا من الرجوع إليه في أي وقت، كما أن إضافة الجدول في أحد ملفات معالجة النصوص مثل ملفات برنامج الوورد تجعل عملية استخدامه أكثر سرعة وسهولة، نظرًا إلى القدرة على إضافة أي بيانات او ملاحظات على الجدول داخل الملف، ولذلك؛ يُمكنكم الحصول على الجدول الدوري للعناصر الكيميائية في ملف بصيغة doc يُمكن إجراء أي تعديل عليه “من هنا“
اقرأ أيضًا: سرعة التفاعلات الكيميائية
شرح الجدول الدوري
عند النظر إلى الجدول الدوري الحديث، سوف أنه يضم مجموعة من المربعات المتعددة التي قد تم ترتيبها وفق دراسات ونظريات وقواعد هامة جدًا وأساسية بالاعتماد على عدد بروتونات النواة في ذرة كل عنصر، ويترتب هذا الجدول في عدد من الدورات التي تأخذ الاتجاه الأفقي ويبلغ عددها سبعة دورات.
في حين أن الترتيب الرأسي للجدول مختلف نوعًا ما؛ حيث أن المجموعات تبلغ ثمانية عشر مجموعة وعدد الإلكترونات في المدار الخارجي لعناصر كل مجموعة متساوي، وعند النظر إلى خواص العناصر، سوف نجد أن المجموعات الأولى من الجدول تضم العناصر الفلزية ثم تبدأ الصفة الفلزية في الانخفاض كلما اتجهنا نحو اليمين مروًا بأشباه الفلزات ووصولًا إلى مجموعة اللافلزات، وفي نهاية الجدول توجد العناصر الخاملة مكتملة المدار الخارجي والتي يتم وصفها بأنها خاملة نظرًا إلى انخفاض الفاعلية الكيميائية لها [3].
وفي نهاية المقال؛ نكون قد عرضنا لكم بالتفصيل كم عدد عناصر الجدول الدوري وأهم خصائص الجدول وشرحه والطريقة الصحيحة التي يُمكن من خلالها استخدام الجدول الدوري الحديث من أجل الوصول إلى مكان أي عنصر بسهولة، ومن ثَم؛ اتمكن من تحديد أهم خصائص هذا العنصر بمجرد النظر إلى موقعه وترتيبه داخل الجدول.
المراجع
- ^ sigmaaldrich , Periodic Table of the Elements , 28/7/2020
- ^ pubchem , Periodic Table of Elements , 28/7/2020
- ^ chemicool , The Periodic Table , 28/7/2020